Klinische Evidenz
Wichtige Indikationen
Bauchspeicheldrüsenkrebs
Bauchspeicheldrüsenkrebs ist weltweit eine der häufigsten krebsbedingten Todesursachen. Die einzige kurative Therapieoption ist die chirurgische Resektion, welche nur in etwa einem Drittel der neu diagnostizierten Fälle sinnvoll möglich ist. Nach Resektion erfolgt eine adjuvante Chemotherapie.
Es liegen Ergebnisse der randomisierten Studie „Hyperthermia European Adjuvant Trial“ (HEAT) vor, welche die regionale Hyperthermie (RHT) mit Cisplatin als Zusatz zu Gemcitabin im Vergleich zur alleinigen adjuvanten Chemotherapie mit Gemcitabin in der ergänzenden Behandlung nach Resektion des Bauchspeicheldrüsenkrebs untersuchte (1).
Insgesamt wurden 117 Patient:innen randomisiert und erhielten im experimentellen Arm an den Tagen 1 und 15 jeweils Gemcitabin 1000 mg/m2 und an den Tagen 2,3 und 16, 17 jeweils Cisplatin 25 mg/m2 mit RHT (n= 57). Im Kontrollarm erfolgte an den Tagen 1, 8 und 15 jeweils Gemcitabin 1000 mg/m2 (n=60). Die adjuvante Therapie erfolgte alle vier Wochen und die Patienten erhielten sechs Behandlungszyklen. Die Studie wurde im Mai 2018 vorzeitig beendet, als das modifizierte FOLFIRINOX-Schema Gemcitabin als Standardtherapie ablöste.
Während die HEAT-Studie keinen signifikanten Unterschied im krankheitsfreien Überleben nachweisen konnte (12,7 vs. 11,2 Monate; p = 0,394), zeigen die Ergebnisse jedoch eine signifikant verbesserte Überlebensrate nach einem Rezidiv im experimentellen Arm (15,3 vs. 9,8 Monate; p = 0,031). Die Rezidivbehandlung erfolgte sekundär vorrangig mit m-FOLFIRINOX oder nab-Paclitaxel plus Gemcitabin, in beiden Studienarmen gleichermaßen. Zudem wurde ein tendenziell besseres Gesamtüberleben von 33,2 vs. 25,2 Monaten (p = 0,099) mit einer 5-Jahres-Überlebensrate von 28,4 % vs. 18,7 % beobachtet. Unerwünschte Ereignisse nach CTCAE-Grad ≥ 3 unterschieden sich nicht signifikant zwischen den Gruppen (61,5 % vs. 63,6 %) und die Toxizität war geringer als mit intensivierter adjuvanter Chemotherapie mit modifiziertem FOLFIRINOX.

Quelle:
Lokoregionär rezidivierender Brustkrebs
Brustkrebs ist weltweit der häufigste Krebs bei Frauen, und ein lokoregionäres Rezidiv kann bei bis zu einem Drittel der zuvor behandelten Patienten auftreten1. Die Behandlung von lokoregionären Brustkrebsrezidiven kann eine Operation und Strahlentherapie oder eine erneute Strahlentherapie bei Patienten umfassen, die sich bereits während der Erstbehandlung einer Strahlentherapie unterzogen haben.
Eine aktuelle Metaanalyse analysierte acht zweiarmige Studien, darunter fünf randomisierte Studien mit insgesamt 627 Patienten, die sich einer Strahlentherapie allein oder einer Strahlentherapie in Kombination mit oberflächlicher mikrowellenbasierter Hyperthermie unterzogen haben1. Die Patienten wurden im Schnitt mit 7 Hyperthermie-Sitzungen behandelt und erreichten eine Durchschnittstemperatur von 42,5 °C. Die mittlere Strahlentherapie-Dosis betrug 38,2 Gy (Bereich 26-60 Gy). Die Hyperthermie wurde am häufigsten nach der Strahlentherapie angewendet. Die komplette Ansprechrate der kombinierten Behandlung betrug 60,2 %, was eine signifikante Verbesserung im Vergleich zu 38,1 % nach alleiniger Strahlentherapie darstellt (odds ratio 2,64; 95%-Konfidenzintervall 1,66-4,18; P<0,0001). Das akute und späte Toxizitätsprofil der kombinierten Behandlung war mild1.
Quelle:
Lokal fortgeschrittener Gebärmutterhalskrebs
Gebärmutterhalskrebs ist die vierthäufigste Krebsart bei Frauen.
Langzeitergebnisse einer randomisierten Studie zum Vergleich der Strahlentherapie mit einer mittleren Gesamtdosis von 68 Gy (einschließlich eines Brachytherapie-Boosts) und insgesamt 5 Sitzungen der regionalen Hyperthermie (42 °C für einen Zeitraum von 60 Minuten) mit einer Strahlentherapie allein bei 114 Patienten mit lokal fortgeschrittenem Gebärmutterhalskrebs liegen vor1. Die Studie zeigte nachhaltige Verbesserungen in ihrem primären Endpunkt, nämlich der lokalen Kontrolle für die kombinierte Behandlung (56 % vs. 37 %; p = 0,01) sowie einer verbesserten Gesamtüberlebenszeit nach 12 Jahren: 37 % vs. 20 % (p = 0,03) mit ähnlichen Spättoxizitätsereignissen der Klasse 3 in beiden Gruppen1.
Für lokal fortgeschrittenen Gebärmutterhalskrebs ist die kombinierte Chemotherapie eine Standardbehandlung. Es ist weniger bekannt, ob die Hyperthermie auch in der Lage ist, die Krebsheilungserfolge der Radiochemotherapie zu verbessern. Daher wird die Kombination von Hyperthermie und Strahlentherapie vor allem für diejenigen Patienten empfohlen, die Kontraindikationen für eine Chemotherapie haben oder nicht bereit sind, sich einer Chemotherapie zu unterziehen.
Eine kürzlich durchgeführte Netzwerk-Meta-Analyse von 59 randomisierten Studien ergab, dass die Kombination aus Hyperthermie und Strahlentherapie im Vergleich zur Chemotherapie bei lokal fortgeschrittenem Gebärmutterhalskrebs gleich wirksam ist2.
Quellen:
Refraktäre oder rezidivierende nicht-testikuläre maligne Keimzelltumore bei Kindern und Jugendlichen
Pädiatrische maligne Keimzelltumore sind selten und machen etwa 3-4 % aller bösartigen Tumore bei Kindern aus, wobei mehr als 50 % bei Säuglingen und Kleinkindern unter 4 Jahren diagnostiziert werden1. Die Polychemotherapie auf Cisplatinbasis führt zu Heilungsraten von bis zu 90 % der Patienten, jedoch haben etwa 10 % der Patienten eine refraktäre oder rezidivierende Erkrankung.
Eine offene, nicht randomisierte monozentrische Phase-2-Studie testete die kombinierte Behandlung mit 3-4 Zyklen Cisplatin-, Etoposid- und Ifosfamid-Chemotherapie (alle angewandt an Tag 1-4) in Kombination mit regionaler Hyperthermie (Tag 1 und 4 jedes Zyklus, 60 Minuten 42 °C) bei 44 Patienten mit refraktären oder rezidivierenden pädiatrischen malignen Keimzelltumoren1. Bei 86 % aller Patienten war ein objektives Ansprechen auf die Behandlung festzustellen. Die ereignisfreie 5-Jahres-Überlebensrate betrug 62 % (95%-KI 45-75), und die 5-Jahres-Gesamtüberlebensrate betrug 72 % (95%-KI 55-83)1. Die Langzeitprognose von Patienten mit schlechtem Ansprechen oder nach einem ersten Rückfall war fast ähnlich wie bei Patienten, die eine Erstbehandlung erhielten, daher deuten die Daten dieser Studie darauf hin, dass Hyperthermie dazu dienen kann, eine vorliegende Chemotherapieresistenz zu überwinden1.
Quelle:
Hochrisiko-Weichteilsarkom
Das Weichteilsarkom ist eine relativ seltene Krankheit, die weniger als 1 % aller Krebsfälle ausmacht. Die Chirurgie und die neoadjuvante oder adjuvante Strahlentherapie stellen den Standard der Behandlung von Hochrisiko-Weichteilsarkomen dar, die perioperative Chemotherapie ist eine zusätzliche Behandlungsoption.
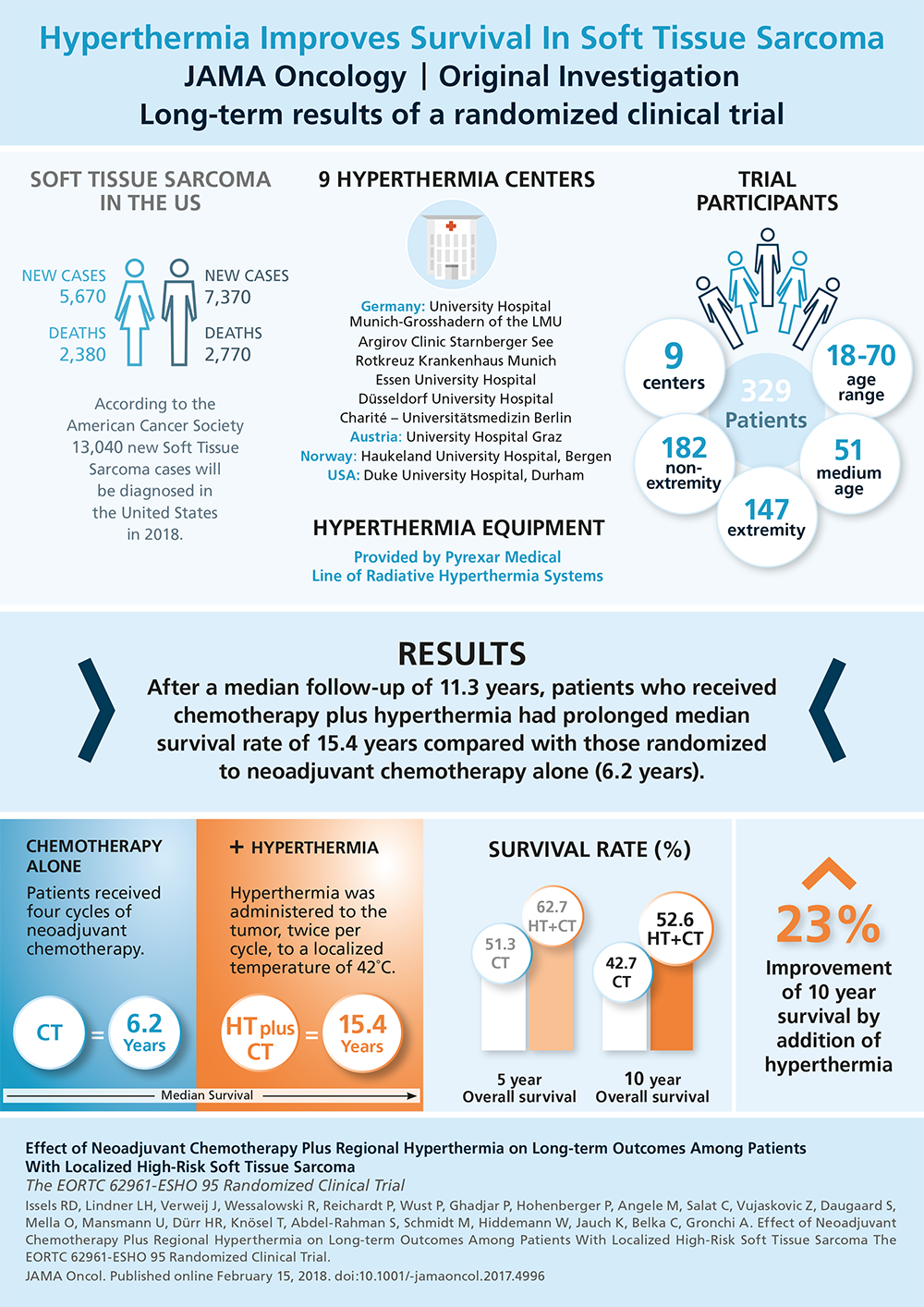
Langzeitergebnisse einer randomisierten Studie liegen vor, in denen die perioperative Chemotherapie (mit Doxorubicin, Ifosfamid und Etoposid, 4 Zyklen Neoadjuvans, 4 Zyklen Adjuvans) sowie die regionale Hyperthermie vs. perioperative Chemotherapie allein bei 341 Patienten mit primärem oder lokal rezidivierendem Hochrisiko-Weichteilsarkom des Rumpfes und der Extremitäten verglichen werden1, 2. Die adjuvante Strahlentherapie wurde mit 50-66 Gy durchgeführt, und es gab keinen Unterschied zwischen den beiden Armen der Studie in Bezug auf die Anwendung der Strahlentherapie. Hyperthermie (42 °C für einen Zeitraum von 60 Minuten) wurde gleichzeitig mit der Verabreichung von Ifosfamid am Tag 1 und 4 jedes Chemotherapiezyklus angewandt. Im Vergleich zur Chemotherapie allein verbesserte die zusätzliche Behandlung mit regionaler Hyperthermie den primären Endpunkt dieser Studie, nämlich das lokale progressionsfreie Überleben (hazard ratio 0,65; 95%-KI 0,49-0,86; P = 0,002). Darüber hinaus war bei Patienten, die mit einer Chemotherapie plus regionaler Hyperthermie behandelt wurden, das Gesamtüberleben verlängert im Vergleich zu denen, die mit einer Chemotherapie behandelt wurden (hazard ratio 0,73; 95%-KI 0,54-0.98; P = .04) mit 5-Jahres-Überlebensratejeweils 62,7% (95%-KI 55,2%-70,1%) vs. 51,3% (995%-KI 43,7%-59,0%) und 10-Jahres-Überlebensrate 52,6% (95%-KI 44,7%-60,6%) vs. 42,7% (95%-KI 35,0%-50,4%) 2.
Quellen:
